Три текущих клинических испытания ELEVIDYS (delandistrogene moxeparvovec-rokl), генной терапии, разработанной Sarepta и продаваемой Roche, были временно остановлены Европейским агентством по лекарственным средствам (EMA). Эта ожидаемая, но не неприятная новость вызвала глубокую печаль в сообществе больных мышечной дистрофией Дюшенна (МДД).
Приостановленные испытания включают исследование Envision фазы 3, спонсируемое Sarepta, в котором оценивается Elevidys у мальчиков в возрасте от 8 до 17 лет; исследование Envol фазы 2 компании Roche, в котором изучается Elevidys у младенцев и новорожденных; и исследование 104 компании Sarepta, в котором проводится исследование фазы 1 Elevidys у мальчиков в возрасте от 4 до 9 лет с уже имеющимися антителами к определенному серотипу.
До Roche, Sarepta и EMA первым сообществом, опубликовавшим это объявление, был наш турецкий партнер >>> DMD Dayanisma.
Компания Roche опубликовала письмо к сообществу, с которым вы можете ознакомиться здесь.PDF)
Оглавление
Почему были остановлены клинические испытания Elevidys?
После смерти 18 марта 2025 года 16-летнего мальчика с мышечной дистрофией Дюшенна, которому была сделана инъекция Elevidys, перспективы генной терапии, которая продается по коммерческой цене $3 млн, резко изменились.Читать далее)
До тех пор, пока не будет установлена точная причина смерти подростка из США, у которого развилась острая печеночная недостаточность (ОПН) после приема Elevidys, Европейское агентство по лекарственным средствам (EMA) потребовало приостановить исследования. Когда пациент скончался в прошлом месяце, Sarepta заявила, что внесет изменения в этикетку Elevidys, включив в нее сигнал безопасности.
SRP-9001-104 Временно приостановлено
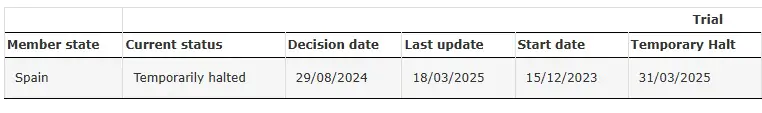
Источник: Клиническое испытание SRP-9001-104
ENVOL (Исследование 302) Временно приостановлено
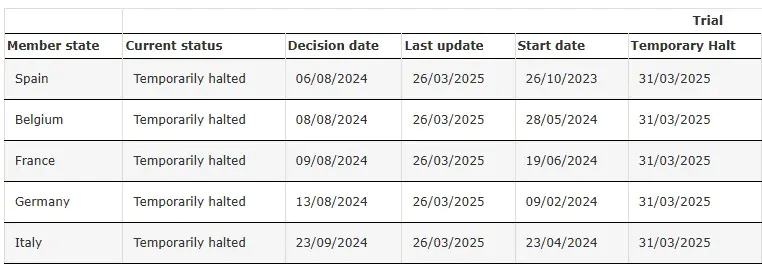
Источник: Клиническое испытание SRP-9001-302
SRP-9001-303 Временно приостановлено
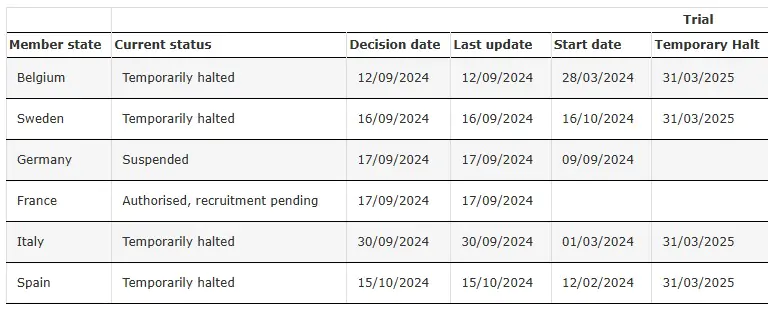
Источник: Клиническое испытание SRP-9001-303
Узнать больше: Представитель DMD WarrioR в Турции делится своими взглядами на генную терапию Elevidys.



https://investorrelations.sarepta.com/news-releases/news-release-details/sarepta-therapeutics-provides-update-elevidys
Sarepta Therapeutics предоставляет (безопасность) обновление ELEVIDYS
04/04/25 8:44 утра по восточному поясному времени
КЕМБРИДЖ, Массачусетс. (BUSINESS WIRE) – 4 апреля 2025 г. – Компания Sarepta Therapeutics, Inc. (NASDAQ:SRPT), лидер в области точной генетической медицины для редких заболеваний, поделилась следующей информацией, касающейся препарата ELEVIDYS (деландистроген моксепарвовек-рокл), единственного одобренного препарата генной терапии для пациентов с мышечной дистрофией Дюшенна.
После обновления безопасности острой печеночной недостаточности, выпущенного 18 марта, органы власти стран-членов Европейского союза (ЕС) запросили, чтобы независимый комитет по мониторингу данных (DMC) провел совещание для рассмотрения неблагоприятного события. Пока анализ завершается, набор и дозирование в некоторых клинических исследованиях ELEVIDYS временно приостановлены.
Независимый DMC собрался 3 апреля и согласился, что на основе совокупности доказательств общий профиль пользы и риска остается благоприятным для продолжения дозирования в приостановленных клинических испытаниях без внесения изменений в протоколы исследований. По запросу регулирующих органов ЕС Sarepta и Roche представят эту информацию в ответ на временную остановку в течение недели. Оценка представления и последующее решение об отмене временной остановки будут следовать за регуляторным процессом ЕС.
Клинические исследования, затронутые временной остановкой, — это исследование SRP-9001-302 (ENVOL), исследование SRP-9001-303 (ENVISION) и исследование SRP-9001-104. Мониторинг и сбор данных для уже зарегистрированных участников продолжаются, и мы не ожидаем существенного влияния на сроки этих исследований.
На фондовом рынке произошло падение акций.
https://dmdwarrior.com/dmd-warriors-turkish-representative-shares-his-views-on-elevidys-gene-therapy-is-it-effective-and-why-is-it-expensive/