أوقفت الوكالة الأوروبية للأدوية (EMA) مؤقتًا ثلاث تجارب سريرية جارية لدواء إيليفيديس (ديلاندستروجين موكسيبارفوفيك-روكل)، وهو علاج جيني طورته شركة ساريبتا وسوّقته شركة روش. وقد أثار هذا الخبر، وإن كان متوقعًا، حزنًا عميقًا لدى مرضى ضمور العضلات دوشين (DMD).
وتشمل التجارب المتوقفة دراسة Envision التي ترعاها شركة Sarepta في المرحلة الثالثة، والتي تقيم Elevidys لدى الأولاد الذين تتراوح أعمارهم بين 8 إلى 17 عامًا؛ ودراسة Envol التي ترعاها شركة Roche في المرحلة الثانية، والتي تبحث في Elevidys لدى الأطفال والمواليد الجدد؛ ودراسة Sarepta's Study 104، وهي نظرة في المرحلة الأولى على Elevidys لدى الأولاد الذين تتراوح أعمارهم بين 4 إلى 9 سنوات مع وجود أجسام مضادة مسبقة لنمط مصل معين.
قبل روش وساريبتا وEMA، كان أول مجتمع ينشر هذا الإعلان هو شريكنا التركي >>> DMD Dayanisma.
وقد أصدرت شركة روش رسالة إلى المجتمع والتي يمكنك قراءتها هنا. (ملف بي دي إف)
جدول المحتويات
لماذا تم إيقاف التجارب السريرية لـ Elevidys؟
بعد وفاة صبي يبلغ من العمر 16 عامًا مصابًا بضمور العضلات دوشين والذي تلقى جرعة من Elevidys في 18 مارس 2025، تغيرت توقعات العلاج الجيني، الذي يتم تسويقه بسعر تجاري قدره $3 مليون دولار، بشكل مفاجئ.اقرأ المزيد)
إلى حين تحديد السبب الدقيق لوفاة مراهق أمريكي أصيب بفشل كبدي حاد (ALF) بعد تناوله دواء Elevidys، طلبت وكالة الأدوية الأوروبية (EMA) تعليق الدراسات. وعندما توفي المريض الشهر الماضي، أعلنت شركة ساريبتا أنها ستُعدّل ملصق دواء Elevidys ليشمل إشارة السلامة.
SRP-9001-104 متوقف مؤقتًا
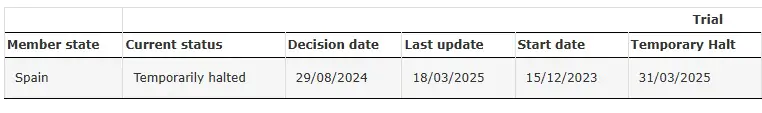
مصدر: التجربة السريرية لـ SRP-9001-104
ENVOL (دراسة 302) متوقف مؤقتًا
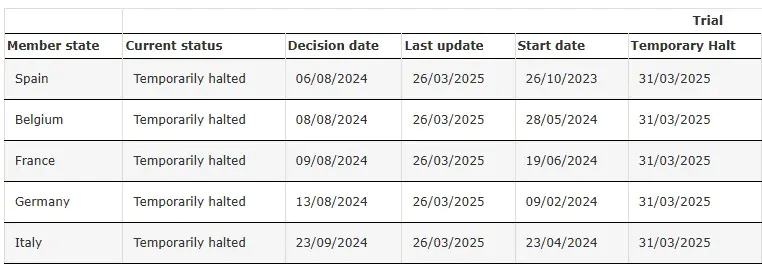
مصدر: التجربة السريرية لـ SRP-9001-302
SRP-9001-303 متوقف مؤقتًا
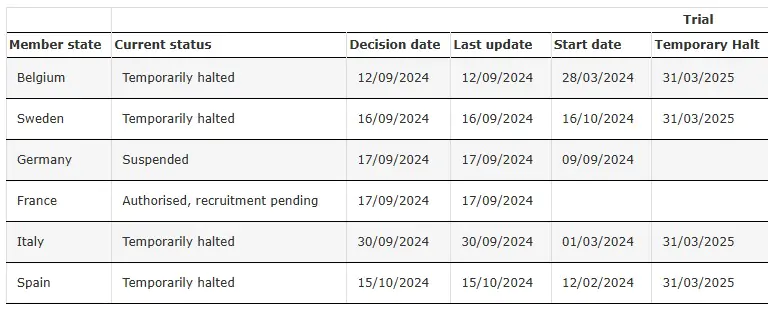
مصدر: التجربة السريرية لـ SRP-9001-303
يتعلم أكثر: ممثل DMD WarrioR التركي يشارك آراءه حول العلاج الجيني Elevidys.



https://investorrelations.sarepta.com/news-releases/news-release-details/sarepta-therapeutics-provides-update-elevidys
Sarepta Therapeutics يوفر تحديثًا (سلامة) على ELEVIDYS
04/04/25 8:44 صباحًا بتوقيت شرق الولايات المتحدة
كامبريدج، ماساتشوستس - (بزنيس واير) - 4 أبريل 2025 - شاركت شركة Sarepta Therapeutics، Inc. (NASDAQ:SRPT)، الرائدة في مجال الطب الجيني الدقيق للأمراض النادرة، التحديث التالي المتعلق بـ ELEVIDYS (delandistrogene moxeparvovec-rokl)، العلاج الجيني الوحيد المعتمد للمرضى الذين يعانون من ضمور العضلات دوشين.
في أعقاب تحديث السلامة بشأن فشل الكبد الحاد الصادر في 18 مارس/آذار، طلبت سلطات الدول الأعضاء المرجعية في الاتحاد الأوروبي اجتماعًا للجنة المستقلة لمراقبة البيانات لمراجعة الآثار الجانبية. وفي انتظار استكمال التحليل، تم إيقاف اختيار المشاركين وتحديد جرعاتهم مؤقتًا في بعض الدراسات السريرية لدواء إيليفيديس.
اجتمعت لجنة إدارة البيانات المستقلة في 3 أبريل/نيسان، ووافقت على أنه بناءً على مجمل الأدلة، يظل نموذج المخاطر والفوائد العام مناسبًا لمواصلة استخدام الجرعات في التجارب السريرية المتوقفة دون أي تغييرات على بروتوكولات الدراسة. بناءً على طلب الجهات التنظيمية في الاتحاد الأوروبي، ستقدم شركتا ساريبتا وروتش هذه المعلومات ردًا على الإيقاف المؤقت في غضون أسبوع. وسيتبع تقييم الطلب والقرار اللاحق برفع الإيقاف المؤقت الإجراءات التنظيمية للاتحاد الأوروبي.
الدراسات السريرية المتأثرة بالتوقف المؤقت هي دراسة SRP-9001-302 (ENVOL)، ودراسة SRP-9001-303 (ENVISION)، ودراسة SRP-9001-104. يستمر رصد المشاركين المسجلين وجمع بياناتهم، ولا نتوقع أي تأثير ملموس على الجدول الزمني لهذه الدراسات.
انخفضت الأسهم في سوق الأوراق المالية.
https://dmdwarrior.com/dmd-warriors-turkish-representative-shares-his-views-on-elevidys-gene-therapy-is-it-effective-and-why-is-it-expensive/