Tres ensayos clínicos en curso de ELEVIDYS (delandistrógeno moxeparvovec-rokl), una terapia génica desarrollada por Sarepta y comercializada por Roche, han sido suspendidos temporalmente por la Agencia Europea de Medicamentos (EMA). Esta noticia, esperada pero no inoportuna, ha causado profunda tristeza en la comunidad de pacientes con distrofia muscular de Duchenne (DMD).
Los ensayos pausados incluyen el estudio de fase 3 Envision patrocinado por Sarepta, que evalúa Elevidys en niños de 8 a 17 años; el estudio de fase 2 Envol de Roche, que investiga Elevidys en bebés y recién nacidos; y el Estudio 104 de Sarepta, una fase 1 que analiza Elevidys en niños de 4 a 9 años con anticuerpos preexistentes a un serotipo particular.
Antes de Roche, Sarepta y EMA, la primera comunidad en publicar este anuncio fue nuestro socio turco >>> DMD Dayanisma.
Roche ha emitido una carta a la comunidad que podéis leer aquí. (PDF)
Tabla de contenido
¿Por qué se detuvieron los ensayos clínicos de Elevidys?
Tras la muerte de un joven de 16 años con distrofia muscular de Duchenne que recibió una infusión de Elevidys el 18 de marzo de 2025, las perspectivas para la terapia génica, que se comercializa a un precio comercial de $3 millones, cambiaron abruptamente.Leer más)
Hasta que se determine la causa precisa de la muerte de un adolescente estadounidense que desarrolló insuficiencia hepática aguda (IAA) tras tomar Elevidys, la Agencia Europea de Medicamentos (EMA) solicitó la suspensión de los estudios. Tras el fallecimiento del paciente el mes pasado, Sarepta anunció que modificará la etiqueta del Elevidys para incluir la advertencia de seguridad.
SRP-9001-104 Suspendido temporalmente
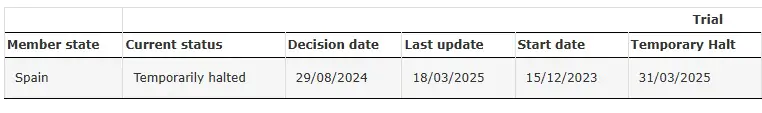
Fuente: Ensayo clínico de SRP-9001-104
ENVOL (Estudio 302) Suspendido Temporalmente
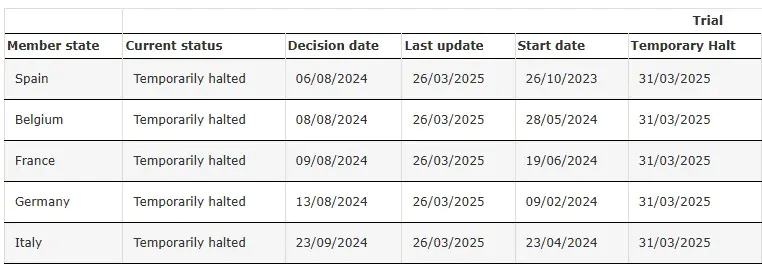
Fuente: Ensayo clínico de SRP-9001-302
SRP-9001-303 Suspendido temporalmente
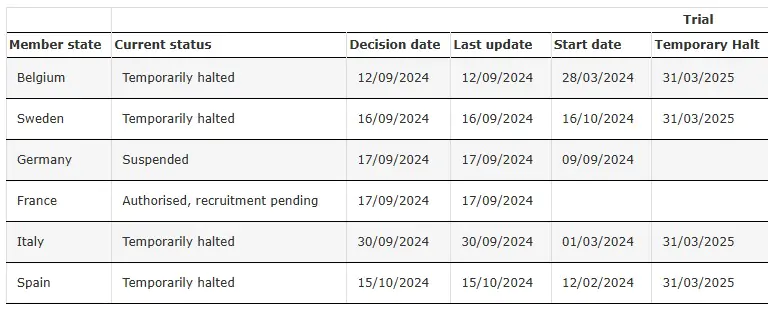
Fuente: Ensayo clínico de SRP-9001-303
Más información: El representante turco de DMD WarrioR comparte sus puntos de vista sobre la terapia genética Elevidys.




https://investorrelations.sarepta.com/news-releases/news-release-details/sarepta-therapeutics-provides-update-elevidys
Sarepta Therapeutics proporciona actualización (de seguridad) sobre ELEVIDYS
04/04/25 8:44 AM EDT
CAMBRIDGE, Mass.–(BUSINESS WIRE)–4 de abril de 2025– Sarepta Therapeutics, Inc. (NASDAQ:SRPT), líder en medicina genética de precisión para enfermedades raras, compartió la siguiente actualización relacionada con ELEVIDYS (delandistrógeno moxeparvovec-rokl), la única terapia génica aprobada en pacientes con distrofia muscular de Duchenne.
Tras la actualización de seguridad sobre la insuficiencia hepática aguda publicada el 18 de marzo, las autoridades de los países miembros de referencia de la Unión Europea (UE) solicitaron que el comité independiente de monitorización de datos (CDM) se reuniera para revisar el evento adverso. Mientras se finaliza el análisis, el reclutamiento y la administración de dosis en ciertos estudios clínicos de ELEVIDYS se suspenden temporalmente.
El DMC independiente se reunió el 3 de abril y coincidió en que, basándose en la totalidad de la evidencia, el perfil beneficio-riesgo general sigue siendo favorable para continuar la dosificación en los ensayos clínicos suspendidos sin modificar los protocolos del estudio. A petición de los reguladores de la UE, Sarepta y Roche presentarán esta información en respuesta a la suspensión temporal en el plazo de una semana. La evaluación de la presentación y la consiguiente decisión de levantar la suspensión temporal se realizarán conforme al proceso regulatorio de la UE.
Los estudios clínicos afectados por la suspensión temporal son el estudio SRP-9001-302 (ENVOL), el estudio SRP-9001-303 (ENVISION) y el estudio SRP-9001-104. El seguimiento y la recopilación de datos de los participantes ya inscritos continúan, y no prevemos un impacto significativo en el cronograma de estos estudios.
Las acciones cayeron en el mercado de valores.
https://dmdwarrior.com/dmd-warriors-turkish-representative-shares-his-views-on-elevidys-gene-therapy-is-it-effective-and-why-is-it-expensive/